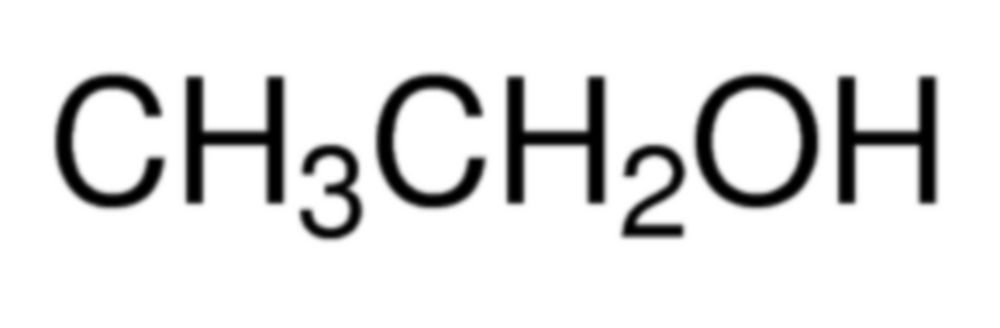Ethanol
Op deze pagina geven we meer informatie over ethanol. Hieronder gaan we het hebben over:
Wat is ethanol?
Ethanol, in de volksmond ook wel alcohol genoemd, is een stof waar de mens al een hele lange geschiedenis mee heeft. Het gebruik van alcohol is dan ook wijdverspreid onder de mensheid. Het woord alcohol is afgeleid van het Arabische woord al-kuḥl (الكحل). Alcoholen zijn een groep van organische verbindingen waarbij een hydroxylgroep (OH) is gebonden aan de koolstofketen. De stof met een keten van twee koolstofatomen, ethylalcohol, is de bekendste en meest voorkomende alcohol, aangezien het een veelgebruikt oplosmiddel is en het de alcohol is die in alcoholische dranken zit. De molecuulformule van ethanol is C2H5OH, vanwege de naam wordt het vaak afgekort als EtOH. Ethanol is een ontvlambare vloeistof met een zoete geur. Er zijn verschillende methoden om ethanol te verkrijgen. Micro-organismen maken ethanol aan tijdens de anaerobe omzetting (fermentatie of vergisting) van bepaalde koolhydraten, dit is het langst bekende proces. In latere tijden slaagde men er ook in ethanol op andere wijze te verkrijgen dan door vergisting. Het is bijvoorbeeld een bijproduct van de raffinage van aardolie. Door zijn desinfecterende eigenschappen wordt ethanol verwerkt in sommige ontsmettingsmiddelen. De chemische industrie gebruikt het bij de synthese van organische verbindingen. Ook veel geneesmiddelen worden met behulp van ethanol toegediend. Ethanol is een belangrijke alternatieve brandstof. De naam Bio-ethanol wordt gebruikt wanneer het uit biologische bronnen wordt gewonnen zoals uit plantaardig materiaal. Bio-ethanol wordt voornamelijk gebruikt als een additief bij benzine
De geschiedenis van ethanol
Fysische eigenschappen van ethanol
Ethanol is een kleurloze, vluchtige vloeistof met een sterke, karakteristieke geur. Onder normale condities brandt het met een rookloze blauwe vlam die niet altijd goed waarneembaar is bij daglicht. De fysische eigenschappen van ethanol vinden voor een groot deel hun oorsprong in de hydroxylgroep en de kleine lengte van de koolstofketen.
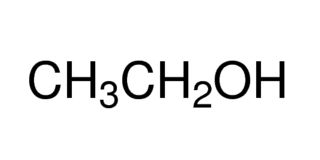
De hydroxylgroep van ethanol neemt deel aan waterstofbindingen, waardoor ethanol minder vluchtig en viskeuzer is dan andere organische verbindingen met een vergelijkbare molaire massa. Als ethanol en water gemengd worden, treedt er een verschijnsel op dat volumecontractie heet; Het volume van het mengsel is altijd kleiner dan de som van de bij elkaar gevoegde volumes. Bij het samenvoegen van gelijke volumes van ethanol en water, blijft er maar 96% van het totaalvolume over van de twee vloeistoffen. De oorzaak van dit verschijnsel is dat water een kleiner molecuul is dan ethanol, waardoor de bijeengevoegde volumes niet simpelweg optelbaar zijn. Het mengen van ethanol en water is exotherm, er ontstaat mengwarmte. Zuivere ethanol is zeer hygroscopisch, dit komt omdat er waterstofbruggen gevormd worden met de watermoleculen die opgenomen worden. De polaire hydroxylgroep zorgt ervoor dat ethanol een goed oplosmiddel voor een groot aantal polaire stoffen, maar omdat ethanol ook over een apolair gedeelte beschikt, kan ethanol ook goed optreden als oplosmiddel voor niet-polaire verbindingen. Mengsels van ethanol en water die meer dan ongeveer 50% ethanol bevatten, zijn ontvlambaar en kunnen makkelijk worden aangestoken.
Toepassingen
Ethanol heeft verschillende toepassingen. Hieronder lichten we er een aantal uit.
Alcohol voor consumptie
Alcoholhoudende dranken worden veel gedronken als sociaal geaccepteerd genotmiddel: bier, wijn, likeur en sterkedrank. Alcohol is een drug die vanwege de fysiek verslavende eigenschappen door sommigen gerekend wordt tot de harddrugs. Toch wordt alcohol wettelijk niet als zodanig gezien. Micro-organismen maken ethanol aan tijdens de anaerobe omzetting (fermentatie of vergisting) van bepaalde koolhydraten. Van oudsher wordt deze gisting gebruikt bij het maken van alcoholische dranken als bier en wijn. Wanneer de oplossing ongeveer 15% ethanol bevat, gaan de gistcellen zelf dood, sterkere alcoholische dranken kunnen alleen op kunstmatige wijze worden geproduceerd. Hiervoor kan men het product destilleren.
Ontsmetten en reinigen
Ethanol bezit een ontsmettende werking. In microbiologische laboratoria wordt een oplossing van 70% ethanol - en 30% water - als ontsmettingsmiddel voor laboratoriumtafels gebruikt. Een hogere concentratie dan 70% heeft minder bacteriedodende werking. Veel reinigingsproducten bevatten alcohol. Alcohol heeft veel kwaliteiten die wenselijk zijn voor een reinigingsmiddel. Het is een goede ontvetter, laat weinig residu achter, en tast ondergronden niet aan. Brandspiritus wordt bijvoorbeeld gebruikt om ruiten schoon te maken. De ethanol is dan vermengd met onder andere methanol en ook een blauwe waarschuwingskleurstof.
Ethanol als brandstof
Ethanol wordt gebruikt als weinig vervuilend additief in brandstoffen als benzine, omdat de verbrandingsproducten relatief schoon zijn. In Brazilië rijden veel auto's op bio-ethanol. Deze bio-ethanol wordt gewonnen uit vergist sap van suikerriet met behulp van destillatie. Watergehalte is de belangrijkste parameter die hierbij onder controle gehouden moet worden. Het natuurlijk evenwicht van een ethanol-wateroplossing is 96% ethanol en 4% water. Bij een hogere concentratie ethanol zal de vloeistof water uit de lucht aantrekken totdat de concentratie het natuurlijke evenwicht weer heeft bereikt. Ethanol die gebruikt wordt in de benzine heeft altijd een concentratie van 99% of meer. Er geldt een Europese bijmengnorm voor watervrije bio-ethanol in benzine. Het relatief hoge gehalte aan reststoffen maakt dat de meeste Bio-ethanol ongeschikt is voor de andere toepassingen. Daarnaast wordt ethanol gebruikt in bijvoorbeeld rechauds en sfeerhaarden.
Vloeistofthermometer
Ethanol wordt gebruikt als hoofdbestanddeel in vloeistofthermometers. Ethanol heeft een erg laag vriespunt, zo'n -115°C, naarmate er meer water aanwezig is in het mengsel gaat het vriespunt omhoog. Vanwege het lage vriespunt kan een alcoholthermometer tot ver onder het vriespunt van water de temperatuur nog aangeven.
Gebruik in de chemie
In het laboratorium wordt ethanol gebruikt bij verscheidene chemische reacties waar een erg sterke base voor nodig is, waaronder eliminatiereacties. Bij reactie met een (aard)alkalimetaal ontstaat namelijk het zeer basische ethoxide-anion en waterstofgas. Ethanol is een bijna universeel oplosmiddel, mengbaar met water in alle verhoudingen, maar daarnaast ook met een grote verscheidenheid aan organische oplosmiddelen, waaronder apolaire stoffen zoals kleinere alkanen, zoals n-pentaan en n-hexaan, ook alifatische halogeenverbindingen zoals trichloorethaan en tetrachlooretheen lossen goed op.
Accijns en Denatureren
Traditiegetrouw wordt er in Nederland belasting geheven op alcohol die geschikt is voor consumptie. Deze belasting is niet van toepassing als het product een ander beoogd gebruik heeft. Daarbij is het wel verplicht dat het product ongeschikt wordt gemaakt voor consumptie door er toevoegingen aan te doen. Dit wordt ook wel denatureren genoemd, de toevoegingen die gedaan moeten worden zijn wettelijk vastgelegd. Vroeger had elk land zijn eigen procedure voor het denatureren, dit had nadelige gevolgen voor in- en export van ethanolhoudende producten.
Sinds 2017 zijn deze toevoegingen op Europees niveau gelijkgetrokken. In het nieuwe systeem wordt onderscheid gemaakt tussen volledig gedenatureerde alcohol en gedeeltelijk gedenatureerde alcohol. Het volledig denatureren heeft als voordeel dat het product vervolgens vrij verhandelbaar is door de hele EU, vrijgesteld van accijns. Hiervoor wordt gebruik gemaakt van Eurodenaturant, dit bestaat uit Isopropylalcohol (IPA), Methylethylketon (MEK) of Denatoniumbenzoaat (Bitrex). Deze stoffen zijn gekozen zodat het voor de consument nagenoeg onmogelijk gemaakt wordt om ze uit de ethanol te halen, Denatoniumbenzoaat is een van de meest bittere stoffen die er bestaat, elk spoor wat achterblijft maakt het product ongeschikt voor consumptie. Andere producten worden gedeeltelijk gedenatureerd omdat de eigenschappen vereisen dat er bijvoorbeeld geen onaangename geur aan zit. Gedeeltelijk gedenatureerde ethanol is vrij verhandelbaar in het land van herkomst maar niet vrij exporteerbaar binnen de EU.
De naam Alcohol Ketonatus komt van oorsprong in de drogisterij branche. Ketonatus verwijst naar de denaturatie met een keton, in Nederland wordt meestal butanon gebruikt, vaak wordt die geur geneutraliseerd door toevoeging van een etherische olie.
Merken ethanol
Als totaalleverancier beschikt Boom over een ruim assortiment ethanol. Naast verschillende zuiverheden bieden we ook veel verschillende verpakkingseenheden bij ons bestellen. Zo hebben we altijd een passende oplossing voor uw wens.

J.T. Baker
Boom beschikt over een ruim assortiment ethanol van het merk J.T. Baker. Een van onze meest verkochte producten is de ethanol 96% 'Baker Analyzed'. Maar we hebben meer opties.

Honeywell
Onder sublabel Riedel-de Haen biedt Honeywell hoge kwaliteit ethanol aan. In Europa is Boom een van de leveranciers van deze toonaangevende leverancier uit de Verenigde Staten.

Boom Ethanol
Onder ons eigen Boom label produceren wij ethanol van verschillende kwaliteiten. U vindt bij ons een ruim assortiment aan ethanol, in diverse verpakkingseenheden.
Ethanol bestellen bij Boom
Bij Boom bieden we een breed assortiment ethanol voor verschillende toepassingen. Dankzij ons diverse aanbod in merken kunnen we ook een ruim aanbod aan ethanol aanbieden. Zo hebben we met elke zuiverheid en verpakkingseenheid altijd een passende oplossing voor uw vraag.Voordelen van bestellen bij Boom: - Meer dan 125 jaar kennis en ervaring
- Persoonlijke aanpak met vaste contactpersonen
- Snelle levering vanuit ons magazijn in Nederland
Bekijk het assortiment ethanol
- Meer dan 125 jaar kennis en ervaring
- Persoonlijke aanpak met vaste contactpersonen
- Snelle levering vanuit ons magazijn in Nederland
Meest verkochte ethanol
Bekijk hier onze meest verkochte ethanol.
Ethanol 96% 'Baker Analyzed'
Basiseenheid:
2,5LT
Artikelnr.
64008007.2500
Merk:
J.T.Baker
Op voorraad
€ 75,90
Bespaar 12% als u er 4 koopt